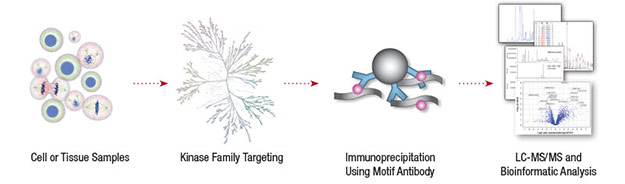
CST 针对非小细胞肺癌 (NSCLC) 中的酪氨酸激酶活性开展了一项整体研究,旨在发现新的致病因素 (1)。磷酸化酪氨酸抗体用于在 LC-MS/MS 分析前,对 41 种 NSCLC 细胞系和 150 种 NSCLC 肿瘤中的磷酸化肽进行富集。该分析在 4551 多个蛋白质上识别出 2700 个磷酸化酪氨酸残基。酪氨酸激酶间变性淋巴瘤激酶 (ALK) 是前 10 种有待后续分析的候选产物之一。
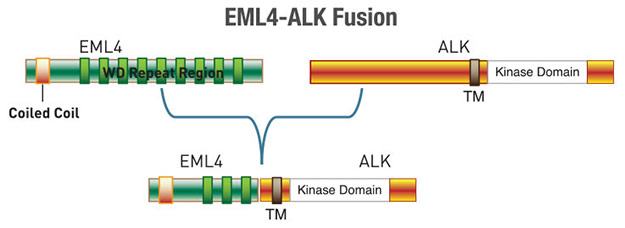
进一步的研究发现,在有某些 NSCLC 细胞系和肿瘤中 EML4(棘皮动物微管结合蛋白样 4)的 N 末端会与 ALK 的 C 末端发生融合。3-7% 的 NSCLC 患者的肿瘤中存在高度易致癌的融合蛋白 (1-4)。表达 EML4-ALK 融合蛋白的癌细胞对于小分子 ALK 抑制剂 Crizotinib 十分敏感,而且在 2011 年美国食品药品监督管理局 (FDA) 已批准将 Crizotinib 用于 ALK 阳性 NSCLC 的治疗 (2)。
CST 开发了一种高特异性和敏感性的抗体 ALK (D5F3®) XP® Rabbit mAb #3633,它可以检测全长 ALK 和 EML4-ALK 融合蛋白。FDA 已批准了免疫组织化学法 (IHC) 伴随诊断测试,此项测试采用了 CST 授权的 ALK D5F3 克隆 (3)。这将帮助医生确定哪些 NSCLC 患者可以采用 Crizotinib 进行有效治疗。
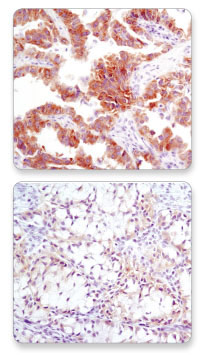
使用 ALK (D5F3®) XP® Rabbit mAb #3633,对具有高水平(上图)与低水平的(下图)ALK 表达的石蜡包埋人类肺癌进行 IHC 分析。