您可以通过点击 CST 信号转导通路图的各个节点查找研究资源或产品信息。您还可以下载通路图,将其用于教育和研究。
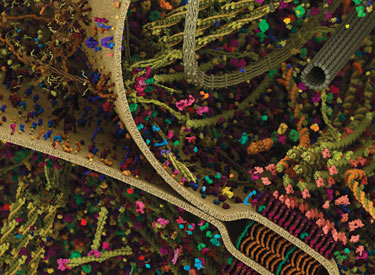
细胞可在其周围环境中与细胞和基质形成许多连接:黏附连接(细胞-细胞)、紧密连接(不渗透的细胞-细胞连接)以及局灶黏附(细胞-基质)。
黏附连接是构成、加强和扩散、降解以及随后重塑的动态结构,因为相关蛋白会与相邻细胞蛋白产生暂时性连接。黏附连接的形成通过钙粘蛋白-链蛋白复合体(由钙粘蛋白、β-链蛋白和 α-链蛋白组成)来介导。细胞连接与细胞骨架之间的连接可能比最初认为的更具动态性,并且可能依赖于钙粘素-链蛋白复合体与肌动蛋白细胞骨架之间的多种微弱联系或依赖于其他膜相关的蛋白(即连接素和肌动蛋白丝结合蛋白)。单体 α-链蛋白在黏附连接处结合 β-链蛋白,并在释放后形成促进肌动蛋白束形成的 α-链蛋白二聚体。支链肌动蛋白网络到束链肌动蛋白纤丝的转变与成熟、较强的黏附连接的形成以及膜板状伪足的减少相关。对于多数动态细胞系统,激酶、磷酸酶和接头蛋白的聚集均可调控一些关键效应蛋白的活性和定位。p120 链蛋白 (δ-链蛋白)可结合质膜上的钙粘蛋白并使其稳定。膜结合和胞质酪氨酸激酶可在微弱或初生连接处磷酸化 β-链蛋白,同时磷酸酶可在已建立的连接处去除 β-链蛋白和 δ-链蛋白上已增加的磷酸根。Rho 家族 GTP 酶可调节连环蛋白和其他重要黏附蛋白的可用性以及激活状态。总的说来,结构蛋白、酶和接头蛋白的聚集组成了形态形成期间短暂结合所必需的动态细胞间连接,并维持了发育后复杂的组织和结构的完整性并促进之后的发育过程。
紧密连接即不渗透的细胞间连接,可在上皮细胞和内皮细胞之间形成一个连续的阻隔液体的屏障。紧密连接可调节细胞旁通透性并维持细胞极性,阻断顶端和基底外侧细胞表面之间跨膜蛋白的运动。紧密连接由密封蛋白和闭合蛋白跨膜蛋白组成,并在与细胞骨架的连接中起作用。闭合蛋白在紧密连接的聚集和维持中至关重要。闭合蛋白在各种残基上的不同磷酸化作用可调节与其他紧密连接蛋白(如 ZO-1)的相互作用。
黏着斑是细胞与细胞外基质之间形成的连接,主要通过整合素进行介导。整合素是 α/β 异二聚体细胞表面受体,该受体在细胞黏附和迁移中具有重要作用。整合素家族至少包含 18 个 α 和 8 个 β 亚基,可形成 24 种已知具有不同组织分布和重叠配体特异性的整合素。整合素的胞内尾端与大量信号转导分子相互作用,包括局灶黏附激酶 (FAK)。通过整合素聚集激活 FAK 会导致在 Tyr397 位点发生自磷酸化,Tyr397 是 Src 家族激酶 PI3K 和 PLCγ 的一个结合位点。